La Regulación de Dispositivos Médicos desde una Perspectiva Dental
Mar 17 de 2023 0
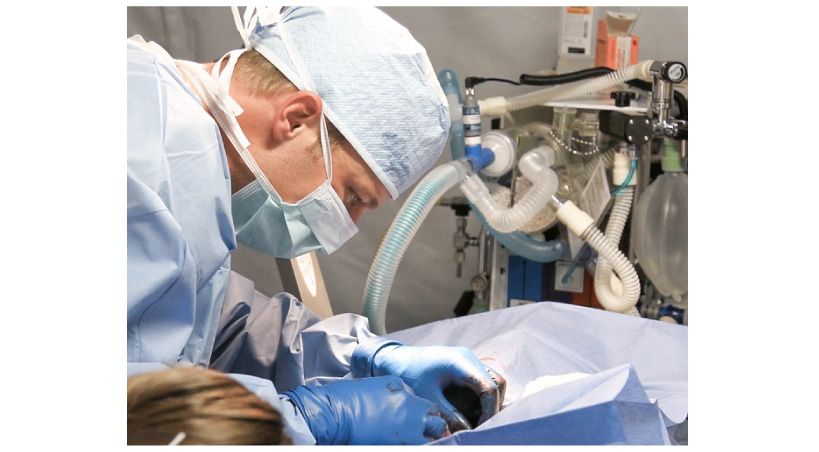
Un nuevo reglamento para la comercialización y aplicación de dispositivos médicos entró en vigor en la Unión Europea a partir de mayo de 2021. Este reglamento se denomina EU 2017/745 o Reglamento de Dispositivos Médicos (MDR). Publicado inicialmente y entró en vigor en 2017, reemplaza la antigua Directiva de Dispositivos Médicos 93/42/EEC (MDD), pero aún está en proceso de modificación. La implicación de esta legislación tiene amplios efectos sobre los fabricantes, importadores, distribuidores, usuarios de dispositivos médicos y pacientes. Este artículo analiza el MDR desde la perspectiva dental. Como se ilustra en este texto, el MDR creará más trámites burocráticos para que los actores industriales obtengan la marca CE (Conformitée Européenne) de sus productos, y más trabajo de documentación para los dentistas. Esto también significa que las empresas más pequeñas que actúan fuera de Europa se ven afectadas de manera desproporcionadamente negativa en comparación con sus contrapartes que actúan a nivel mundial. El MDR podría y muy probablemente dará como resultado una reducción considerable y un aumento de precio de los productos que están disponibles para los dentistas europeos. Además, el MDR podría crear una brecha entre los científicos de materiales dentales que trabajan en las universidades y la industria dental, porque esta última ahora tiene que destinar más dinero a los asuntos regulatorios en lugar del desarrollo o la innovación de productos. Por otro lado, el MDR también puede actuar como un antetipo para regulaciones similares en otras partes del mundo y podría ofrecer nuevas oportunidades de carrera para personas en investigación de materiales dentales, especialmente en el campo regulatorio.
La versión final y formateada del artículo se publicará pronto.
Fuente: Frontiers in Dental Medicine